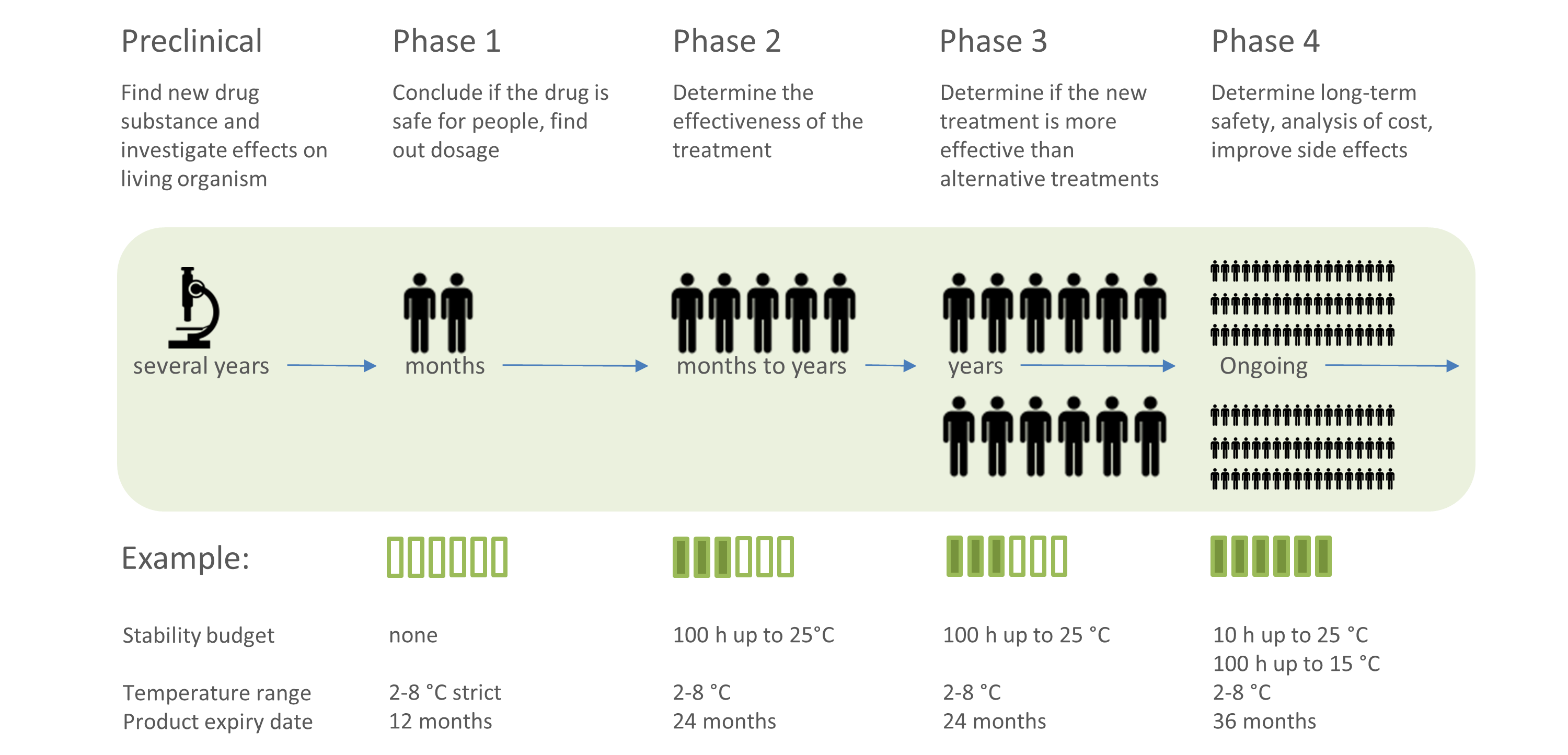
Das Einmaleins der Kühlketten-Überwachung
Erfahren Sie mehr darüber, wie Sie Ihre temperaturgeführte Lieferkette verwalten können. Erhalten Sie einen Überblick in die Überwachung der Kühlkette und entdecken Sie Themen wie Stabilitätsbudget, Mean Kinetic Temeprature und mehr!